Actuellement, moins d’un « candidat médicament » sur dix entrant en phase d’essais cliniques est au final commercialisé. Ce phénomène entraîne des délais de mise sur le marché de plus en plus longs et une augmentation des coûts de développement. Cependant, la tendance pourrait s’inverser grâce à l’identification précoce des candidats médicaments présentant la meilleure efficacité et une toxicité minimale en évaluant leur comportement in vivo (chez l’animal mais aussi chez l’Homme) dès les toutes premières phases de conception. Une technique consiste à « étiqueter » ces molécules en substituant certains atomes (H, C, F…) par leurs isotopes (stables ou radioactifs). On obtient alors des molécules dites marquées qui sont détectables dans l’organisme. Ainsi, l’hydrogène (H), présent dans toutes les molécules organiques utilisées en santé humaine, peut être remplacé par le deutérium (stable) ou le tritium (radioactif).
La synthèse de molécules marquées rapide, peu coûteuse et utilisant des techniques respectueuses de l’environnement, est aujourd’hui un grand défi en chimie isotopique. En effet, l’introduction de deutérium ou de tritium sur une position définie d’une molécule d’intérêt nécessite généralement le recours à des précurseurs chimiques et à une construction en plusieurs étapes.
Une équipe du CEA-IBITECS, en collaboration avec un laboratoire associant INSA1, le CNRS et l’Université Paul Sabatier (Toulouse), a mis au point une méthode de marquage par « activation C-H ». Cette méthode, réalisable en conditions douces, est applicable à des molécules complexes et fragiles et utilise des nanoparticules de ruthénium. Les chercheurs ont travaillé sur l’échange isotopique d’une liaison C-H, dans le cas où l’atome de carbone est chiral, c’est-à-dire lorsqu’il porte quatre groupements différents. Un carbone chiral n'est pas superposable à son image dans un miroir (Il en est de même pour nos deux mains). La très grande majorité des médicaments et des molécules d’intérêt comporte ce type de carbone. Les chercheurs ont réussi à démontrer l’exceptionnel potentiel des nanoparticules de ruthénium à réaliser un échange isotopique sur un carbone chiral sans modifier la structure tridimensionnelle initiale de la molécule. En parallèle de ces résultats, les chercheurs ont mené une étude de chimie computationnelle qui a permis de dévoiler le mécanisme réactionnel tout à fait original de ce procédé. Ce dernier ouvre de nouvelles perspectives tant chimiques que biologiques et permet d’imaginer de nouveaux développements en matière de marquage, applicables aussi bien à la recherche fondamentale qu’à la chimie des médicaments ou des matériaux.
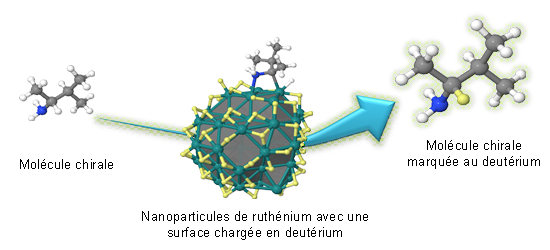
Echange isotopique entre la nanoparticule de ruthénium (dont la surface est imprégnée en deutérium) et le carbone chiral permettant un marquage de la molécule sans modifier sa structure tridimensionnelle initiale. © Romuald Poteau (CNRS) et Grégory Pieters (CEA).
- Institut National des Sciences Appliquées de Toulouse