BRCA1, découvert il y a plus de 20 ans, est un gène prédisposant au cancer du sein et de l'ovaire, qui code pour une protéine impliquée dans la réparation par recombinaison homologue des cassures d'ADN. Avec l'avènement des technologies de séquençage ADN, de nouveaux variants de ce gène sont identifiés quotidiennement chez des patientes. La moitié des mutations de ces variants ne génèrent pas de codon stop prématuré, qui induirait une perte de fonction certaine de la protéine tronquée. Ces variants restent donc classés comme des variants de signification inconnue (VUS). Cette inconnue empêche d'adapter le suivi de la patiente et de ses proches.
La classification des VUS constitue un défi majeur pour le diagnostic de la prédisposition au cancer du sein et de l'ovaire. Plus de 1 000 VUS déjà identifiés doivent être classés, chacun représentant un travail indépendant. La complexité fonctionnelle de la protéine BRCA1 est telle que les outils de classification in silico sont insuffisants.
Cette étude vise à identifier expérimentalement l'impact de grands ensembles de VUS BRCA1 sur le risque de cancer. Pour cela, les équipes ont mesuré de manière systématique les défauts de structure, de liaison aux partenaires et de fonction de réparation de l'ADN de 78 variants BRCA1, dont 65 VUS (variants issus de la base de données française UMD-BRCA1/BRCA2) (Figure 1). Ces variants présentent une mutation dans la région codant pour les domaines BRCT, domaines qui reconnaissent des peptides phosphorylés des protéines partenaires de BRCA1.
|
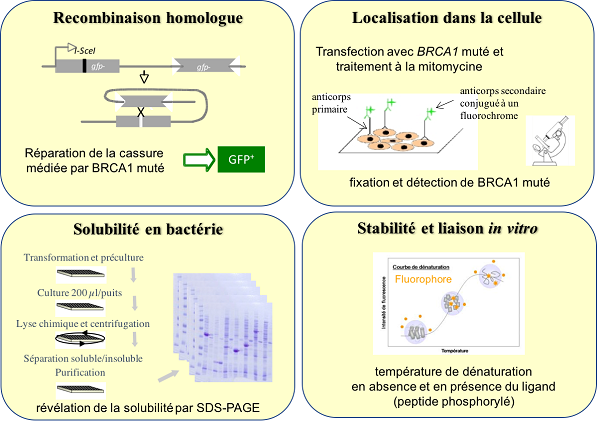
Figure 1 : Schéma de la stratégie expérimentale mise en place pour caractériser les 78 variants de BRCA1 étudiés. Ces expériences ont permis d'évaluer la localisation cellulaire et la capacité à contribuer à la réparation par recombinaison homologue des dommages de l'ADN de chaque variant de la protéine BRCA1 (figures du haut). Elles ont permis de mesurer la solubilité en bactérie, la stabilité et la capacité à lier des peptides phosphorylés cibles des domaines BRCT de chacun de ces variants BRCA1 (figures du bas).
|
Cette analyse a montré que la plupart des variants contrôle, déjà classifiés comme causaux par des études épidémiologiques, présentaient un défaut de solubilité lorsqu'exprimés en bactérie et un défaut d'activité de réparation par recombinaison homologue des dommages de l'ADN en cellules humaines. De plus, tous les variants causaux testés n'interagissaient plus que faiblement avec leurs peptides phosphorylés cibles, alors qu'aucun variant contrôle neutre ne montrait un tel défaut.
Ces résultats permettent de proposer (Figure 2) :
- que les VUS déficients en réparation de l'ADN et qui présentent, en outre, des domaines BRCT insolubles dans les bactéries ou défectueux pour la liaison aux phosphopeptides, entraînent une augmentation du risque de cancer ;
- que les variants ayant une activité de réparation normale et dont les domaines BRCT se lient avec une affinité normale aux 5 phosphopeptides testés sont neutres.
Le cas des variants ayant une activité de réparation normale et une liaison aux phosphopeptides défectueuse devra être caractérisé davantage, car ce dernier défaut fonctionnel pourrait être suffisant en soi pour provoquer la tumorigenèse.
|
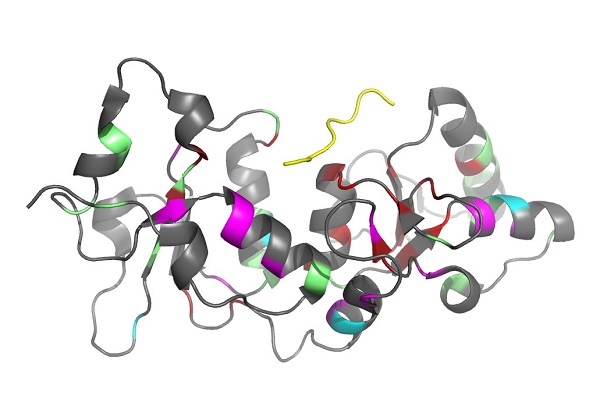
Figure 2 : Structure tridimensionnelle des domaines BRCT de la protéine BRCA1 (en gris) en complexe avec un peptide d'un partenaire (en jaune). Les acides aminés mutés dans les 78 variants analysés sont colorés sur la structure de BRCA1 : 13 variants contrôle étudiés, déjà classés comme causaux (rouge) ou neutres (cyan) à partir de données épidémiologiques ; variants de signification inconnue classés comme potentiellement causaux à partir des expériences de cette étude en rouge également ; variants évalués dans cette étude comme potentiellement neutres en vert ; variants non classés en magenta. Il apparaît clairement qu'un grand nombre de variants mutés dans la région proche du peptide sont causaux (rouges), ce qui suggère fortement l'importance d'un défaut de liaison au peptide dans le processus de cancérogenèse.
|
La problématique abordée ici sur les VUS BRCA1 est emblématique des difficultés d'interprétation rencontrées par les généticiens face à l'explosion du séquençage de nouvelle génération. Des approches expérimentales telles que celle de la présente étude pourront très certainement constituer une aide précieuse pour la prise en charge des familles des patientes.