Un point de départ : la maladie de la vache folle
L'expérience du
Service de Pharmacologie et Immuno-analyse (SPI,
DMTS) dans le développement de tests de détection rapide ne date pas d'hier. L'histoire commence au milieu des années 90. En 1996, la communauté scientifique apporte la preuve que l'agent pathogène responsable de la maladie de la vache folle (une encéphalopathie spongiforme, maladie neurodégénérative) – le prion – peut se transmettre à l'homme et provoquer l'apparition d'un variant de la maladie Creutzfeldt-Jacob. Le SPI, et plus particulièrement le laboratoire LERI à Saclay, a l'expérience nécessaire en matière de tests de dépistage immunologique pour développer,
en collaboration étroite avec l'unité de Dominique Dormont au
CEA de Fontenay-aux-Roses (actuellement le
SEPIA à l'Institut de Biologie François-Jacob), un kit de détection rapide du prion. La mise au point va vite. Et lorsque l'Union européenne lance un appel d'offre pour le développement de tels tests, le CEA est déjà en mesure de répondre. Leur test sera
validé en 1999 et sera
commercialisé par la société Bio-Rad.
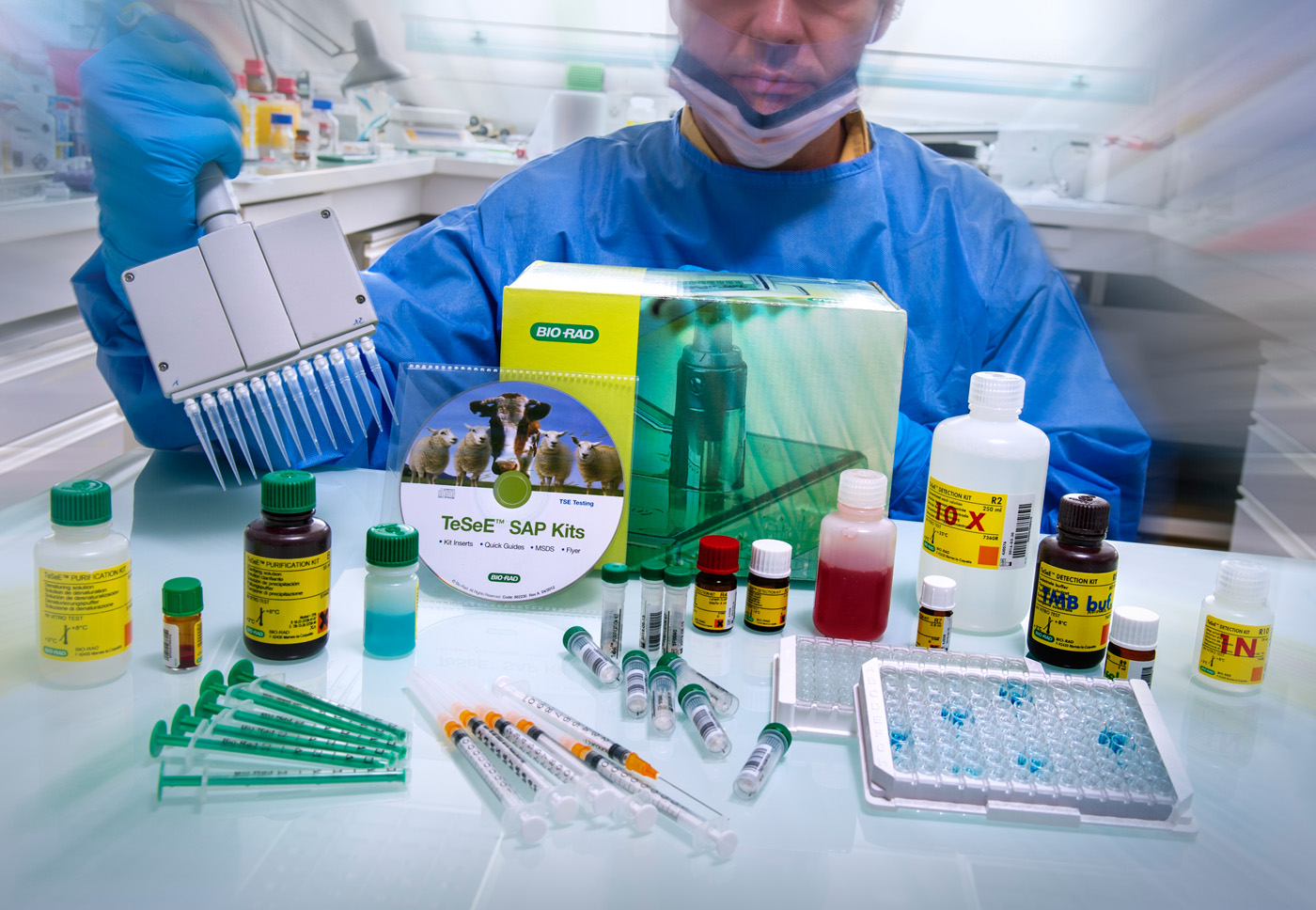
Kit de détection utilisé dans les abattoirs d’Europe, sur les bovins de plus de 24 mois pour détecter la présence ou non du prion, agent responsable de la maladie de la vache folle développé au CEA et commercialisé par Bio-Rad. © L. Godart/CEA
L’expérience du programme NRBC-E
En 2005, l’Etat confie au CEA la responsabilité d’un programme interministériel de recherche et développement contre le terrorisme NRBC-E (nucléaire, radiologique, biologique, chimique et explosive). Ce programme et piloté par le CEA/DAM et fait intervenir l’ensemble des directions opérationnelles du CEA. Le SPI met alors au point des outils d’immuno-analyse performants pour détecter et quantifier certains des agents pathogènes responsables de la menace biologique. Deux laboratoires du SPI, le LERI à Saclay et le
LI2D (ex-LICB) à Marcoule montent très vite en compétence et sont capables de développer des tests contre différents types d’agents pathogènes, que ce soit des virus, des bactéries ou des toxines.
La flambée d'Ebola en 2014 : encore une réussite diagnostique
Alors que l'épidémie d'Ebola est considérée par l'Organisation Mondiale de la Santé comme une « urgence de santé publique de portée internationale », les chercheurs du LI2D (ex LICB), le laboratoire du SPI situé à Marcoule, réussissent l'exploit de mettre au point un test de détection rapide du virus Ebola moins de quatre mois après l'alerte de l'OMS.
Ebola eZYSCREEN®, c'est son nom, est le premier test marqué CE IVD[1] développé au CEA en collaboration avec un industriel normand dans un format proche de celui d'un test de grossesse.
L'antibiorésistance, un autre front
L'antibiorésistance, enjeu de santé publique majeure avec la
dissémination de bactéries multi-résistantes (BMR), constitue l'un des axes forts de développement de tests au LERI. La lutte contre cette dissémination
en milieu hospitalier nécessite une identification rapide des patients porteurs afin de mettre en place des mesures d'hygiène renforcées et d'administrer un traitement approprié le plus précocement possible. En étroite collaboration avec NG BIOTECH et l'AP-HP, le LERI a déjà développé et validé
trois tests rapides de détection d'antibiorésistance.
Et aujourd'hui ?
Forts de leur savoir-faire, les laboratoires du CEA-Joliot souhaitent
développer et pérenniser une filière française de tests immunologiques de diagnostic rapide in vitro de maladies émergentes ou ré-émergentes ou d'agents de la menace biologique pour répondre rapidement, voire
anticiper de futures crises sanitaires. Depuis 2015, leur collaboration avec NG BIOTECH et l'AP-HP s'intensifie :
- Fin 2019, le
LERI et
NG BIOTECH créent un
laboratoire commun pour rechercher, développer, produire et commercialiser une nouvelle génération de tests de détection de l'antibiorésistance.
- En 2020, au tout début de la pandémie de COVID-19, les partenaires (LERI, LI2D, NG BIOTECH et AP-HP)
se mobilisent pour répondre aux enjeux de la pandémie avec la réalisation d'un test rapide sérologique validé dès fin la fin du mois de mars.
- En 2022, les mêmes obtiennent un financement pour leur projet
DiagRaMIE dans le cadre de l'appel à manifestation d'intérêt « Maladies infectieuses émergentes (MIE) et menaces nucléaires, radiologiques, biologiques et chimiques (MN) » de
Stratégie nationale d'accélération déployée dans le cadre du plan
France Relance et du
PIA4. DiagRaMIE vise avant tout à développer de nouveaux anticorps et des tests rapides contre des agents pathogènes identifiés comme menace.
Dernier exemple en date,
le LI2D et NG BIOTECH développent actuellement un test antigénique rapide permettant la détection du Monkeypox virus et le diagnostic de la variole du singe qui touche aujourd'hui plusieurs pays sur plusieurs continents. Des
premiers tests prototypes, avec d'excellentes performances en termes de sensibilité sur du virus en culture, sont en cours d'évaluation dans un laboratoire de haute sécurité biologique du LI2D.

Evaluation des premiers prototypes de tests de détection du virus Monkeypox dans un laboratoire de haute sécurité biologique du LI2D à Marcoule. © CEA
Contact CEA-Joliot :
[1] Le marquage CE est « l'engagement visible du fabricant que son produit respecte les exigences réglementaires en vue de sa libre circulation sur l'ensemble du territoire de l'Union européenne » (Direction générale des entreprises). Le marquage CE IVD concerne les dispositifs médicaux de diagnostic
in vitro.